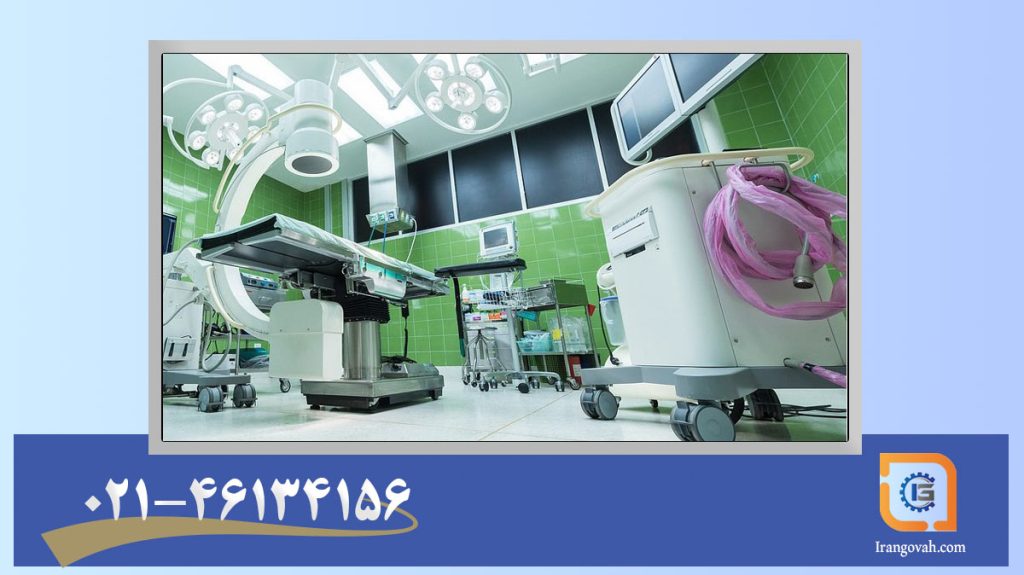
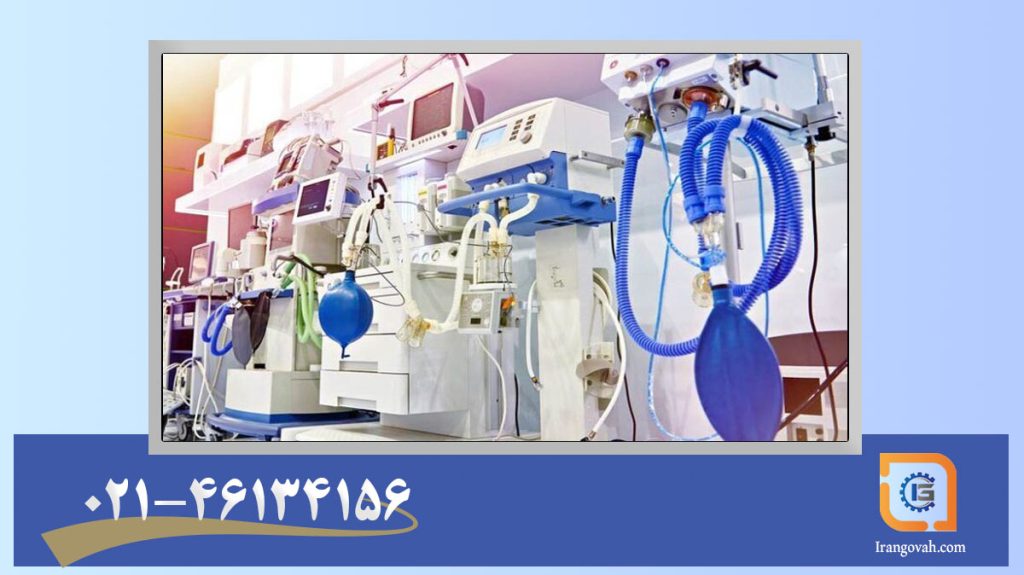
QMS برای صنعت تجهیزات پزشکی (راهنمای عملی ۲۰۲۵–۲۰۲۶)
آخرین بهروزرسانی: ۷ سپتامبر ۲۰۲۵ خلاصهٔ مدیریتی نیاز به مشاوره دارید؟ با ما تماس بگیرید… ۰۲۱-۴۶۱۳۴۱۵۶ ۰۲۱-۴۶۱۳۲۲۹۷ QMS چیست و چرا در تجهیزات پزشکی حیاتی است؟ QMS مجموعهای یکپارچه از سیاستها، فرآیندها، رویهها و سوابق است که کیفیت، ایمنی و انطباق مقرراتی را در کل چرخهٔ عمر محصول تضمین میکند—از طراحی تا پسازعرضه (PMS). برای […]
QMS برای صنعت تجهیزات پزشکی (راهنمای عملی ۲۰۲۵–۲۰۲۶) مطالعه بیشتر »